Cuando el trauma traspasa generaciones: la ciencia detrás de la memoria celular
¿Y si las hambrunas, guerras y persecuciones que sufrieron nuestros antepasados hubieran dejado cicatrices no solo en la historia, sino en tu propio cuerpo? La ciencia está explorando una idea revolucionaria: el trauma puede heredarse, dejando marcas a través de la EPIGENÉTICA. (Lehrner & Yehuda, 2018).
Después del descubrimiento de la epigenética vemos muchas cosas con otros ojos, nos alejamos de la idea del determinismo genético, es decir, la creencia de que nuestros comportamientos eran controlados totalmente por el ADN.
Aunque tengamos un solo código genético, la epigenética nos dice cómo este código es usado (y en palabras más técnicas, cómo es expresado). Todas nuestras células tienen el mismo ADN y los mismos genes, pero no funcionan igual: una neurona y una célula del hígado son muy distintas porque expresan genes diferentes. Según Ghai y Khader (2021) la epigenética controla estos cambios mediante:
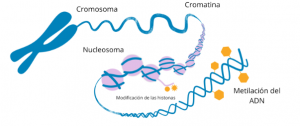
- La metilación del ADN: añade unas marcas que son unos grupos metilos que controlan qué genes se activan o silencian, casi como un interruptor.
- Remodelación de la cromatina: la cromatina es una forma de organización del ADN y la remodelación consiste en “abrir” o “cerrar” el ADN para facilitar que las proteínas lean los genes).
Figura 1. Mecanismos epigenéticos, traducción al español de Álvarez (2021)
Y aquí nos preguntamos ¿Pueden estos cambios heredarse? Respuesta corta, sí. Se solìa pensar que el epigenoma (el manual de modificaciones para controlar tus genes) de un embrión estaba nuevo de paquete, sin estrenar; pero hoy sabemos que algunas modificaciones se heredan, este fenómeno es llamado herencia epigenética (The University of Utah, 2009).
Pero en este artículo estamos debatiendo la relación de la herencia del trauma y la epigenética. Así que primero hay que considerar que el concepto de trauma depende del contexto. Para la medicina un trauma es una lesión física; para los psicologìa es un choque emocional con un daño duradero; y podemos decir que la epigenética redefine el trauma como una forma extrema de adversidad social (Dubois & Guaspare, 2020).
El fenómeno que habla sobre que las experiencias traumáticas de generaciones pasadas pueden influir el comportamiento o emociones de generaciones futuras se conoce como trauma intergeneracional. El trauma puede desencadenar modificaciones epigenéticas que cambien la expresión de nuestros genes y esto puede ser heredado. Había evidencia de que en una generación inmediata después de un trauma de hambruna como en Rusia durante el asedio de Leningrado (Stanner et al., 1997), o en China durante la gran hambruna china (Song et al., 2009); podrían provocar enfermedades como esquizofrenia, diabetes o enfermedades coronarias en la adultez; pero no había evidencia de trauma intergeneracional. Como es difícil y poco ético construir experimentos con humanos para probar traumas de hambrunas se planteó el uso de un organismo modelo: Caenorhabditis elegans, un nemátodo bastante usado para estudios genéticos.
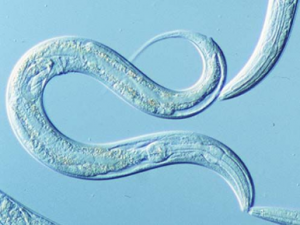
Figura 2. Caenorhabditis elegans (Society for mucosal immunology, 2014)
Este estudio del 2014 usó a Caenorhabditis elegans para estudiar si la inanición podría afectar a la herencia y qué tan duraderos eran estos efectos. Se encontró que se heredan ARN pequeños (small RNA o sRNA), ARNs que regulan genes, y estos afectaban genes que participaban en la nutrición del nemátodo. Incluso la tercera generación después de provocar hambruna en estos organismos mostraba un tiempo de vida más largo, o sea, vivían más.
El siguiente esquema muestra el resumen del experimento:
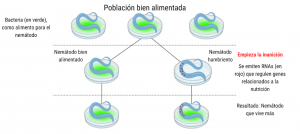 Figura 3. Resumen del experimento (Adapatado de Rechavi et al., 2014 )(Creado en BioRender y Canva)
Figura 3. Resumen del experimento (Adapatado de Rechavi et al., 2014 )(Creado en BioRender y Canva)
Estudios en humanos, como el de Yehuda et al. (2016), mostraron que hijos de sobrevivientes del Holocausto presentaban estos “interruptores químicos” (metilación) en el gen FKBP5, que está relacionado al estrés. Estos cambios, aunque no alteran la secuencia del ADN, pueden afectar cómo se expresan los genes relacionados con la respuesta al estrés y la salud mental. Sin embargo, la transmisión transgeneracional (más allá de la segunda generación) sigue siendo controvertida, ya que factores ambientales y genéticos también influyen. (Ghai & Kader, 2021)
Los investigadores creen que el trauma podría programar células reproductivas (espermatozoides u óvulos). Por ejemplo, en animales, el estrés en el padre altera ciertas moléculas (microARNs) en esperma, afectando el desarrollo cerebral en las crías. En humanos, se ha visto que la violencia durante el embarazo produce cambios en el gen del receptor de glucocorticoides (NR3C1) en los hijos. No obstante, se necesitan más investigaciones para descartar que el entorno influye y confirmar si estos efectos persisten en generaciones no expuestas. (Ghai & Kader, 2021)
La evidencia, desde los “interruptores” químicos activados en hijos de sobrevivientes del Holocausto hasta las moléculas alteradas en las células reproductivas de animales estresados, nos sugiere que el trauma pueden estar presente biológicamente en la siguiente generación. Pero, el conocimiento completo de esta herencia sigue siendo un misterio. Mientras los científicos trabajan para descifrar cuánto se debe a la epigenética y cuánto al entorno que nos rodea, nos enfrentamos a una pregunta: ¿estamos destinados a cargar con las cicatrices biológicas de nuestros antepasados, o comprender este mecanismo nos dará la clave para sanar el futuro?
Bibliografía
- Ghai, M., Kader, F. A Review on Epigenetic Inheritance of Experiences in Humans. Biochem Genet 60, 1107–1140 (2022). https://doi.org/10.1007/s10528-021-10155-7
- Álvarez, L. (2021). Modeling epigenetic evolutionary algorithms: An approach based on the epigenetic regulation process. arXiv (Cornell University). https://doi.org/10.48550/arxiv.2102.09634
- Lehrner A, Yehuda R. Cultural trauma and epigenetic inheritance. Development and Psychopathology. 2018;30(5):1763-1777. doi:10.1017/S0954579418001153
- Dubois, M., & Guaspare, C. (2020). From cellular memory to the memory of trauma: Social epigenetics and its public circulation. Social Science Information, 59(1), 144-183. https://doi.org/10.1177/0539018419897600
- The University of Utah. (2009). Epigenetics & Inheritance. https://learn.genetics.utah.edu/content/epigenetics/inheritance/
- Society for mucosal immunology. (2014). An Overview of the Model Organism: C. Elegans.
- Rechavi, O., Houri-Ze, L., Anava,m S., Yen, S., Hannon, G., Hobert, O. (2014). Starvation-Induced Transgenerational Inheritance of Small RNAs in C. elegans. Cell. Volumen 158. https://www.cell.com/cell/fulltext/S0092-8674(14)00806-X?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS009286741400806X%3Fshowall%3Dtrue
- Rechavi, O., Houri-Ze’evi, L., Anava, S., Goh, W. S. S., Kerk, S. Y., Hannon, G. J., & Hobert, O. (2014). Starvation-Induced Transgenerational Inheritance of Small RNAs in C. elegans. Cell, 158(2), 277–287. https://doi.org/10.1016/j.cell.2014.06.020
- Song, S., Wang, W., and Hu, P. (2009). Famine, death, and madness: schizophrenia in early adulthood after prenatal exposure to the Chinese Great Leap Forward Famine. Soc. Sci. Med. 68, 1315–1321.
- Stanner, S.A., Bulmer, K., Andre` s, C., Lantseva, O.E., Borodina, V., Poteen, V.V., and Yudkin, J.S. (1997). Does malnutrition in utero determine diabetes and coronary heart disease in adulthood? Results from the Leningrad siege study, a cross sectional study. BMJ 315, 1342–1348.